Preguntas Frecuentes de los Tratamientos de Plasma y Anticuerpos Monoclonales
¿Qué tratamientos de anticuerpos existen?
Escuchará acerca de los anticuerpos en relación a los siguientes tratamientos:
Tratamientos con anticuerpos monoclonales
Transfusión directa con plasma convaleciente de COVID (CCP por sus siglas en inglés)
Globulina hiperinmune (HIG por sus siglas en inglés)
¿Qué son los anticuerpos monoclonales (mAbs)?
Los anticuerpos monoclonales (mAbs por sus siglas en inglés) son anticuerpos creados en laboratorios que ayudan al cuerpo a combatir enfermedades específicas. Los tratamientos han sido recibidos en Estados Unidos y han demostrado que disminuyen hospitalizaciones y mejoran los resultados en pacientes de alto riesgo. Funcionan como anticuerpos sustitutos cuando el cuerpo no está produciendo los propios. Imitan la capacidad del sistema inmunológico para combatir agentes dañinos como el virus que causa el COVID-19.
El tratamiento de anticuerpos monoclonales ya está disponible en todo el país. Se administra a pacientes recién diagnosticados que no han sido hospitalizados.
El sistema inmunológico detecta y destruye virus como el que causa COVID-19, el SARS-CoV-2. Una manera en que el sistema inmunológico del cuerpo ataca a un virus es produciendo una gran cantidad de anticuerpos. Estos anticuerpos se adhieren a una proteína o molécula específica que causa una enfermedad llamada antígeno. Una vez adheridos, los anticuerpos pueden obligar a otras partes del sistema inmunológico a destruir las células que contienen el antígeno.
El término anticuerpo monoclonal significa que se clona un anticuerpo artificial y se dirige a un antígeno específico. (Los anticuerpos policlonales se sintetizan a partir de diferentes células inmunitarias y los anticuerpos producidos se unen a múltiples antígenos).
Las empresas Regeneron, Eli Lilly y GlaxoSmithKline fueron autorizados para el uso de emergencia de sus tratamientos de anticuerpos monoclonales. Estos medicamentos están diseñados para bloquear la unión viral y la entrada a las células humanas, neutralizando así el virus que causa COVID-19.
Estos y otros 11 tratamientos experimentales con anticuerpos monoclonales están siendo sometidos a pruebas en humanos, con al menos otros 150 anticuerpos en investigación de descubrimiento. Lea más sobre estos al hacer clic aquí.
Hay información disponible sobre anticuerpos monoclonales.
Información para médicos.
¿Quién puede recibir tratamiento con anticuerpos monoclonales?
Requisitos Generales de Elegibilidad del Paciente para Tratamientos Monoclonales:
Prueba viral directa POSITIVA para SARS-CoV-2 (Antígeno o PCR, rápida o no rápida)
Estar dentro de los 10 DÍAS del inicio de los síntomas
12 años de edad o más, que pesen al menos 40 kg (88 libras) y que estén en ALTO RIESGO de progresar a COVID-19 grave
ALTO RIESGO se define por un mínimo de uno de los siguientes. Otras afecciones o factores médicos (por ejemplo, raza o etnia) también pueden colocar a los pacientes individuales en alto riesgo de progresar a COVID-19 grave y la autorización del tratamiento según la EUA no se limita a las afecciones o factores médicos que se enumeran a continuación. Para obtener información adicional sobre las afecciones médicas y los factores asociados con un mayor riesgo de progresar a un COVID grave, consulte el sitio web de los CDC. Los proveedores de atención médica deben considerar el beneficio-riesgo para un paciente individual.
Edad avanzada (por ejemplo, edad ≥65 años), o
Obesidad o sobrepeso (por ejemplo, IMC> 25 kg / m2, o si tiene entre 12 y 17 años, tiene un IMC ≥ 85 percentil para su edad y sexo según las tablas de crecimiento de los CDC), o
El embarazo o
Diabetes o
Enfermedad inmunosupresora o tratamiento inmunosupresor, o
Enfermedad cardiovascular (incluida la cardiopatía congénita) o hipertensión, o
Enfermedades pulmonares crónicas (por ejemplo, enfermedad pulmonar obstructiva crónica, asma [moderada a grave], enfermedad pulmonar intersticial, fibrosis quística e hipertensión pulmonar), o
Enfermedad de células falciformes, o
Trastornos del neurodesarrollo (por ejemplo, parálisis cerebral) u otras afecciones que confieren complejidad médica (por ejemplo, síndromes genéticos o metabólicos y anomalías congénitas graves), o
Tener una dependencia tecnológica relacionada con la medicina (por ejemplo, traqueotomía, gastrostomía o ventilación con presión positiva (no relacionada con COVID 19))
Este tratamiento NO ESTÁ autorizado a pacientes que:
fueron hospitalizados a causa de COVID-19, o
necesiten terapia de oxígeno a causa de COVID-19, o
que requieran un aumento en el flujo de oxígeno a causa de COVID-19 en aquellos que reciban terapia de oxígeno crónica debido a una comorbilidad no relacionada con COVID-19.
¿Dónde puedo recibir el tratamiento?
Haga clic aquí para un listado de ubicaciones.
¿Si no califico para el tratamiento, qué puedo hacer?
Si usted no califica para el tratamiento, considere unirse a un ensayo clínico.
Para saber más sobre los ensayos clínicos acerca de mAb, visite www.riseabovecovid.org, O
Ensayos clínicos de Eli Lilly: trials.lillytrialguide.com / blaze2study.com/ , O
Ensayos clínicos de Regeneron: https://www.regeneron.com/covid19.
¿Qué Anticuerpos Monoclonales han sido aprobados para el uso de emergencia?
Casirivimab e Imdevimab
El producto de Regeneron consta de dos anticuerpos monoclonales que se dirigen a diferentes proteínas de pico. Casirivimab e Imdevimab se administran juntos por infusión intravenosa (IV) o inyección, según el proveedor, para el tratamiento de COVID-19, leve a moderado, en pacientes adultos y pediátricos. Se recomienda que este tratamiento se administre lo antes posible después de una prueba viral positiva para SARS-CoV-2 y dentro de los 10 días posteriores al inicio de los síntomas.
Más información detallada sobre este tratamiento está disponible aquí.
Ficha técnica para médicos. Ficha técnica para pacientes.
La información en español está disponible aquí.
Bamlanivimab y Etesevimab
El producto de Eli Lilly consta de dos anticuerpos monoclonales que se dirigen a diferentes proteínas de pico. Bamlanivimab y Etesevimab se administran juntos por infusión intravenosa (IV) para el tratamiento de COVID-19, leve a moderado, en pacientes adultos y pediátricos. Se recomienda que este tratamiento se administre lo antes posible después de una prueba viral positiva para SARS-CoV-2 y dentro de los 10 días posteriores al inicio de los síntomas.
Más información detallada sobre este tratamiento está disponible aquí.
Ficha técnica para médicos. Ficha técnica para pacientes.
La información en español está disponible aquí.
Sotrovimab
El producto de GlaxoSmithKline consisa de un anticuerpo monoclonal que está específicamente dirigido contra la proteína de pico del SARS-CoV-2 y está diseñado para bloquear la unión del virus y su entrada en las células humanas. Se administra por infusión intravenosa (IV) para el tratamiento de COVID-19 leve a moderado en pacientes adultos y pediátricos. Se recomienda que este tratamiento se administre lo antes posible después de una prueba viral positiva para SARS-CoV-2 y dentro de los 10 días posteriores al inicio de los síntomas.
Ficha técnica para médicos. Ficha técnica para pacientes.
Puede leer más sobre los diferentes tratamientos en:
¿Hay alguien a quien pueda llamar para hacer más preguntas?
Los proveedores de atención médica o los pacientes que necesiten ayuda para localizar un sitio de infusión o conectarse con un ensayo clínico pueden llamar al Centro de atención telefónica de terapia con anticuerpos monoclonales de ASPR. Inglés: 877-332-6585 Español: 877-366-0310.
¿La terapia de anticuerpos protege contra variantes virales?
Ciertas variantes del virus del SARS-CoV-2 circulante pueden asociarse con resistencia a los anticuerpos monoclonales. Casirivimab / Imdevimab fabricado por Regeneron está disponible para su uso en todos los estados. El producto de Eli Lilly, Bamlanivimab / Etesevimab, ya no se distribuye a AZ, CA, FL, IN, OR y WA debido a preocupaciones sobre la resistencia de variantes. A marzo de 2020, las dosis de bamlanivimab solo se administran con dosis de etesevimab. La información actualizada sobre las autorizaciones de uso de emergencia (EUA por sus siglas en inglés), están disponibles por la Administración de Alimentos y Medicamentos en los Estados Unidos (FDA por sus siglas en ingles).
Ciertas variantes circulantes del virus del SARS-CoV-2 pueden asociarse a la resistencia hacia los anticuerpos monoclonales. Debido al aumento en general de las variantes resistentes al bamlanivimab solamente, el gobierno de EE. UU. detuvo la distribución de bamlanivimab exclusivamente a partir del 24 de marzo de 2021. Bamlanivimab será combinado con etesevimab para el tratamiento de infusión, el cual ha demostrado ser más efectivo. También se utilizan casirivimab e imdevimab. La información actualizada sobre las autorizaciones de uso de emergencia (EUA por sus siglas en inglés), están disponibles por la Administración de Alimentos y Medicamentos en los Estados Unidos (FDA por sus siglas en ingles).
Las variantes de COVID son evidentes en los EE. UU. y se rastrean mediante secuenciación genética (tasas de variante por estado). Aunque la información de secuenciación es útil a nivel de población, los resultados de cada paciente no se comunican al proveedor, al laboratorio remitente o al paciente. La secuenciación del genoma completo no está actualmente aprobada para su uso como prueba de diagnóstico para tomar decisiones sobre el tratamiento de cada paciente. Además, el tiempo de respuesta para este tipo de prueba es tardado, lo cual significa que no es adecuado para decisiones de tratamiento que involucran anticuerpos monoclonales, que deben administrarse lo antes posible una vez que el paciente ha desarrollado síntomas y pruebas positivas. Los tratamientos con anticuerpos, administrados en etapa temprana, siguen siendo la única opción para los pacientes con COVID-19 recién diagnosticados y no hospitalizados.
¿Cómo son administrados los tratamientos de anticuerpos monoclonales a un paciente?
Los tratamientos de anticuerpos monoclonales son administrados por infusión o inyección (solo REGEN-COV). Dado que muchos centros de infusión a menudo tratan a otros pacientes con sistemas inmunitarios en riesgo, los centros deben tener mucho cuidado para garantizar que los pacientes que tienen COVID-19 no entren en contacto con otros pacientes inmunodeprimidos, como los que tienen cáncer. Las infusiones se pueden administrar solo en entornos en los que los proveedores de atención médica tienen acceso inmediato a medicamentos para tratar una reacción grave a la infusión, como reacciones alérgicas y la capacidad de activar el sistema médico de emergencia, según sea necesario. Estos requisitos limitan la cantidad de ubicaciones que pueden proporcionar mAb a los pacientes con COVID.
Si un hospital no cumple con estos requisitos, no debe ofrecer este tratamiento. Si un hospital recibe un cargamento de mAb y no lo puede aplicar de manera segura, estas dosis son entregadas a otra institución que pueda usarlas.
En Junio 2021, se aprobó el tratamiento por inyección, lo que debería aumentar el número de lugares que ofrecen tratamientos con anticuerpos.
¿Se pueden usar los anticuerpos monoclonales para prevenir el COVID-19?
No. Estos medicamentos no están autorizados para usarse como prevención contra el COVID-19.
Si recibo el tratamiento de anticuerpos monoclonales, ¿aún necesito usar cubrebocas y practicar el distanciamiento social?
¡Sí! Todos los días y de cualquier manera. Por favor no ponga en riesgo la salud de las demás personas por su propia comodidad.
¿Dónde puedo encontrar más información sobre la historia y la ciencia detrás de los anticuerpos monoclonales?
Para obtener información, visite aquí y aquí. También hay un foro de discusión en este enlace.
¿Qué es la terapia de plasma convaleciente (CCP)?
CCP es plasma extraído de una persona que se ha recuperado de COVID-19. Cuando esta contagiado, su cuerpo crea anticuerpos para combatir la enfermedad. Estos anticuerpos se desarrollan en su plasma sanguíneo. Cuando el plasma rico en anticuerpos de una persona es transferido a otra persona, esto puede ayudar a iniciar la respuesta inmune y ayudar en la recuperación.
Hable con su doctor sobre el tratamiento con CCP. CCP está disponible a las personas que están hospitalizadas con COVID-19, y las últimas investigaciones muestran que el tratamiento es más eficaz cuando se administra lo antes posible.
El 1 de septiembre, 2020 la Administración de Medicamentos y Alimentos (FDA por sus siglas en inglés) autorizó de emergencia el uso de plasma convaleciente de COVID-19 como tratamiento para pacientes hospitalizados con COVID-19. La información para médicos interesados en obtener plasma para sus pacientes está disponible aquí. Información adicional para pacientes y familiares está disponible aquí. Su médico debe colaborar con el banco de sangre u hospital para obtener plasma.
Puede tener acceso a plasma convaleciente al inscribirse en un ensayo clínico que continuará a rastrear la seguridad y eficacia de los tratamientos CCP. Algunos pacientes han sido reclutados para participar en estos estudios en diferentes instalaciones médicas. Para recibir el tratamiento de plasma, debe ingresar a un ensayo médico supervisado o recibir permiso a través de una autorización de emergencia. La lista de ensayos y más información la encuentra aquí.
Para más información sobre anticuerpos y plasma, consulte nuestra otra lista de preguntas frecuentes.
Aprender sobre las opciones de tratamiento de covid.
¿Qué es la globulina hiperinmune?
La globulina hiperinmune (HIG por sus siglas en inglés) es un producto concentrado fabricado de miles de unidades de plasma convaleciente de miles de donadores. Una asociación sin precedentes de líderes de la industria está trabajando en conjunto para rápidamente y de manera segura desarrollar, probar y producir este tratamiento derivado del plasma, que concentra los anticuerpos del plasma a un medicamento. La distribución equitativa y el fácil acceso a la HIG es una prioridad. En este tiempo, el acceso a la HIG es únicamente posible a través de algunos ensayos clínicos. Aprenda más sobre HIG aquí.
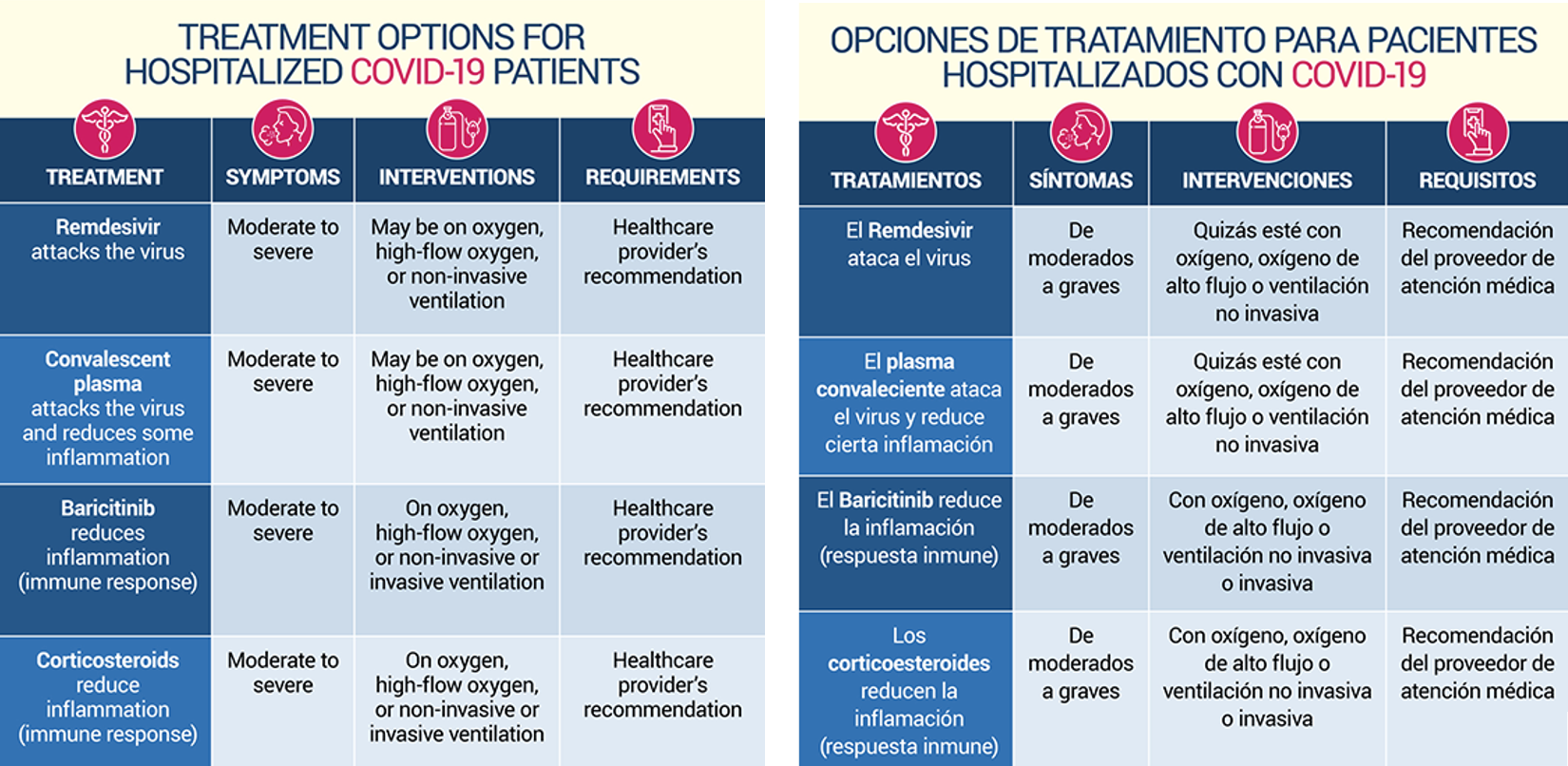
¿Existen otras opciones de tratamientos contra el COVID-19?
Se están utilizando otros tratamientos para tratar el COVID y se están estudiando aún más. En este momento, los tratamientos a continuación se están utilizando para tratar el COVID en un entorno hospitalario o bajo el cuidado de un médico. Aprender sobre las opciones de tratamiento de COVID. Además, la FDA ha autorizado el uso de emergencia del dispositivo de estimulación del nervio vago, gammaCore Sapphire CV, para uso en el hogar o en un entorno de atención médica. Ayuda a tratar pacientes adultos con COVID que experimentan una situación agravada de la disnea relacionada con el asma y un flujo de aire reducido y para quienes no toleran las terapias con medicamentos aprobados o no brindan el suficiente alivio de los síntomas. Más información está disponible aquí.
Información adicional sobre tratamientos está disponible, aquí.